| 复肿章真、朱骥教授团队CinClare研究问鼎JCO:基因引导下新辅助放化疗将局部晚期直肠癌pCR率翻一番 | 您所在的位置:网站首页 › 肿瘤ccr pcr › 复肿章真、朱骥教授团队CinClare研究问鼎JCO:基因引导下新辅助放化疗将局部晚期直肠癌pCR率翻一番 |
复肿章真、朱骥教授团队CinClare研究问鼎JCO:基因引导下新辅助放化疗将局部晚期直肠癌pCR率翻一番
|
中华医学会放射治疗专业委员会常委 CSCO放射治疗专委会副主委 上海医学会放疗专委会候任主任委员 上海市抗癌协会放疗专委会主委 上海市领军人才 NCI直肠癌工作组成员
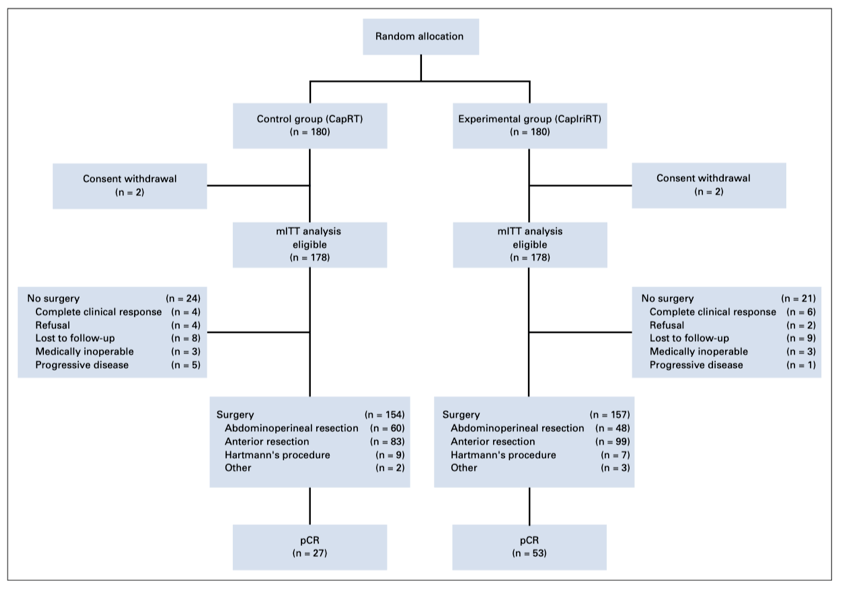
朱骥 主任医师,硕士生导师,肿瘤学博士,流行病与卫生统计学硕士 复旦大学附属肿瘤医院放射治疗科主任医师 CSCO生物统计专家委员会副主任委员 CSCO青年专家委员会常委 CACA大肠癌专业委员会放疗学组副组长、青委会委员 中国外科医师协会MDT专委会青委会副主任委员 中华医学会临床流行病分会循证医学学组委员 中国中西医结合学会普外专委会直肠癌防治专家委员会常委 上海市抗癌协会放射治疗专委会秘书长/青委会副主任委员 上海市医学会放射治疗专委会青委会副主任委员 上海市医学会临床流行病分会委员 研究背景及目的 作为新辅助放化疗的联合用药,伊立替康的疗效早已有了相关报道,但由于担心患者的耐受性差而限制了伊立替康的广泛应用。有研究报道,尿苷二磷酸葡萄糖醛酸转移酶1A1(UGT1A1)基因型是影响伊立替康剂量的关键因素。因此,CinClare研究旨在探究新辅助放化疗同期联用伊立替康的疗效,这也是首个在UGT1A1基因型指导下,将伊立替康联用于局部晚期直肠癌新辅助放化疗的Ⅲ期临床试验。 研究方法 这是一项在中国17个中心开展的随机、开放标签、多中心的Ⅲ期临床试验。 入选标准为:患者年龄在18~75岁之间,经组织病理学确认为直肠腺癌,肿瘤距离肛门≤10cm,盆腔磁共振(MRI)显示肿瘤的临床分期为cT3~4和/或N+,常规的胸部和腹部CT扫描未见远处转移。其他的纳入标准包括Karnofsky评分≥70;所有患者均接受UGT1A1基因型的检测,并确定基因型为*1*1或*1*28型;骨髓造血功能及肝肾功能正常。主要的排除标准为:除外皮肤基底细胞癌或原位宫颈癌的恶性肿瘤史;既往接受过化学治疗或盆腔放疗;怀孕或哺乳期女性;患有二氢嘧啶脱氢酶缺乏症以及在过去的12个月内出现过严重疾病,如不稳定性心绞痛或心肌梗塞。 研究方案:对照组(CapRT)接受盆腔调强放疗(50 Gy / 25次),同期口服卡培他滨(825 mg/m 2 /d,bid,d1~5),放化疗结束后2周采用卡培他滨加奥沙利铂(XELOX)化疗1程(奥沙利铂130 mg/m 2 ,d1,卡培他滨1000 mg/m 2 ,bid,d1~14)。试验组(CapIriRT)接受50 Gy/25次盆腔放疗,同期口服卡培他滨(625 mg/m 2 /d,bid,d1~5),每周接受1次伊立替康化疗,并在放化疗完成后2周进行卡培他滨加伊立替康(XELIRI)方案化疗(伊立替康200 mg/m 2, d1,卡培他滨1000 mg/m 2 ,bid,d1~14)。值得注意的是,研究者根据患者的UGT1A1的基因型对患者的伊立替康周化疗剂量进行了调整,对于UGT1A1* 1 * 1的患者,伊立替康的剂量为80 mg/m 2 ,而UGT1A1 * 1 * 28型患者的剂量为65 mg/m 2 。放化疗完成后8周进行手术,术后均采用5个周期的XELOX方案辅助化疗。 统计分析:研究预计将pCR率从CapRT组的12%提升至CapIriRT组的25%,主要研究终点为意向治疗(ITT)人群的pCR率。次要终点包括毒性、生活质量、肿瘤消退等级、括约肌保存、手术并发症、局部控制、无病生存期(DFS)和总生存期(OS)。 研究计划招募360例合格患者,双侧检验水平α=0.05,检验效能为85%。由于部分患者接受全新辅助治疗后拒绝接受手术,因此,研究者计划进行两次敏感性分析以确认结果的稳健型,包括手术人群的pCR率和ITT人群的完全缓解(CR)[病理完全缓解(pCR)+临床完全缓解(cCR)]率。对肿瘤退缩良好且拒绝根治手术的患者采取“观察等待”策略(watch-and-wait policy)。具体的策略包括:6个周期的巩固化疗,每1~2个月进行直肠指检,每3个月进行一次胸部和腹部CT以及盆腔MRI检查。将cCR定义为放化疗后至少12个月,直肠指检未触及肿瘤,盆腔MRI或肠镜检查无肿瘤残留且肿瘤持续消失。 研究结果 2015年11月至2017年12月,中国共17个中心招募了360例患者,4例因撤回知情同意被排除,共356例患者组成了改良的ITT(mITT)人群(图1)。表1显示了两组患者的基线信息和临床特征。
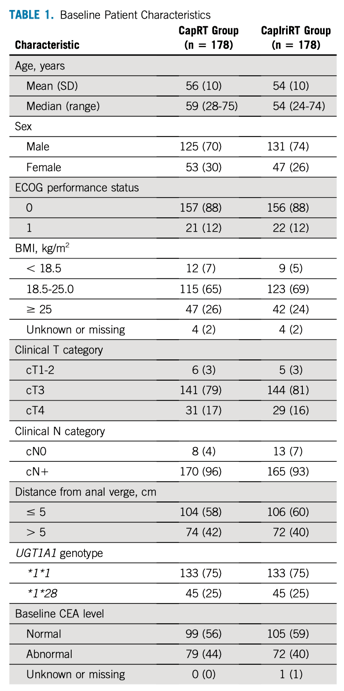
图1. CinClare研究的CONSORT图 表1. 入组患者基线特征
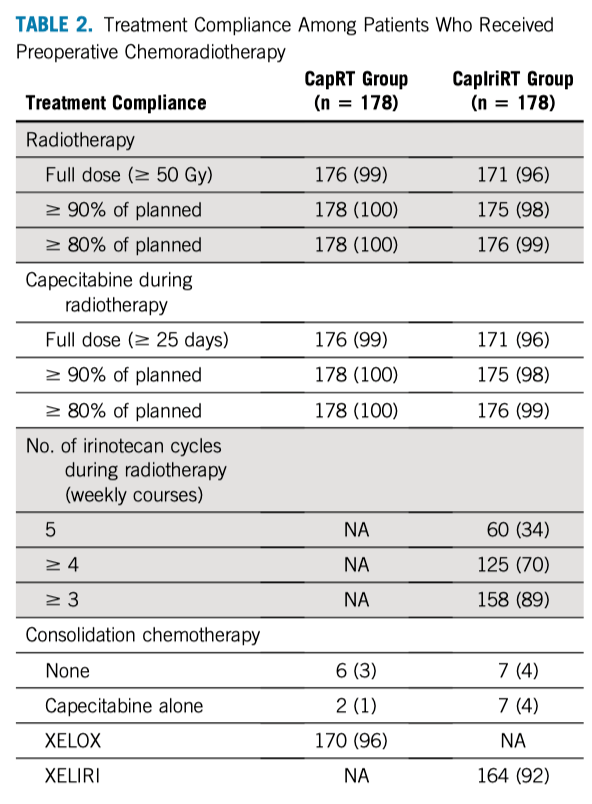
新辅助放化疗的依从性与毒性 CapRT组所有(100%)患者都接受了≥90%的放疗和卡培他滨计划剂量治疗。在CapIriRT组中,有175例(98%)患者接受了≥90%的放疗和卡培他滨计划剂量治疗,125例(70%)患者接受了至少4个周期的伊立替康周化疗(表2)。 表2. 患者接受新辅助治疗的依从性
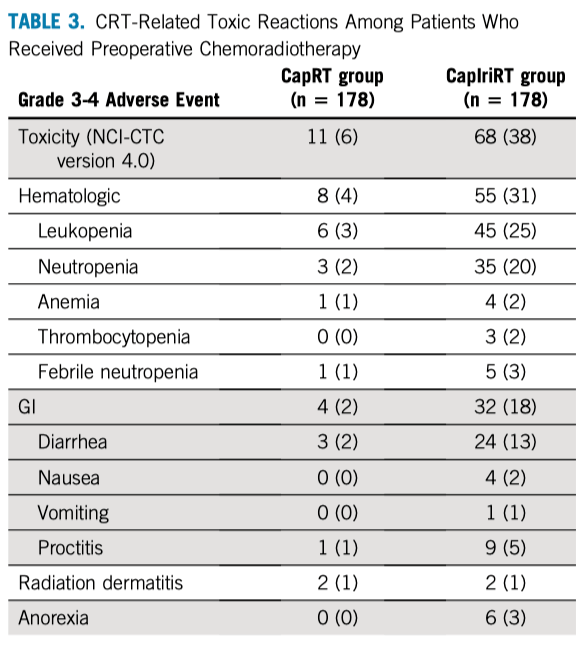
CapRT组和CapIriRT组3~4级毒性反应的发生率分别为6%和38%( P< 0.001)。两组在放化疗期间最常见的3~4级毒性分别是白细胞减少症(3% vs 25%),中性粒细胞减少症(2% vs 20%)和腹泻(2% vs 13%)(表3)。 表3. 新辅助放化疗的毒性反应发生率
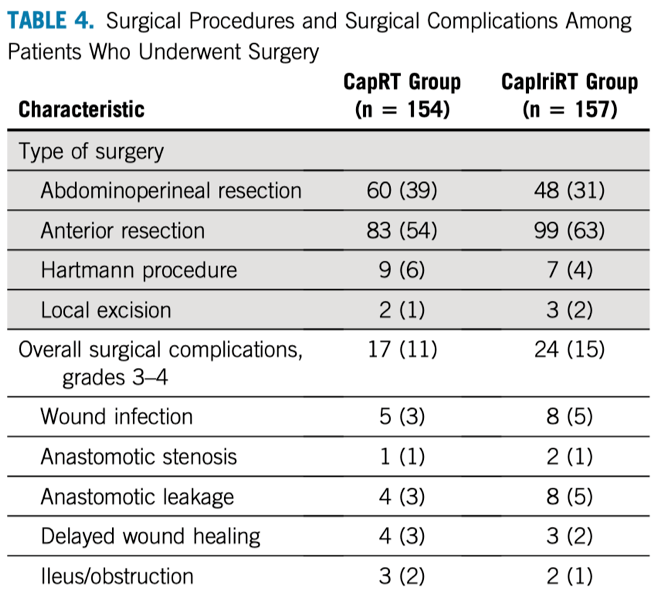
手术及病理结局 CapRT组和CapIriRT组各有154例(87%)和157例(88%)患者接受了手术。CapRT组放化疗结束至手术的中位间期为61天(范围 45~104天),CapIriRT组为62天(范围 4~156天)。CapRT组和CapIriRT组患者接受腹会阴联合切除术(APR)的比例分别为39%和31%( P = 0.120),两组术后出现3级以上并发症的患者比例相似(11% vs 15%; P= 0.268),手术后60天内均无患者死亡。见表4。 表4. 手术患者的手术类型及术后并发症情况
CapRT组中有148例患者(96%)接受了根治手术,CapIriRT组有153例(97%),两组分别有7例(5%)和3例(2%)患者的环切缘≤1 mm。CapRT组和CapIriRT组分别有27例(18%)和53例(34%)患者达到了pCR( HR= 1.93; P< 0.001)。两组的淋巴结阴性率分别为73%和74%。在mITT人群中,CapRT组的pCR率为15%,CapIriRT组为30%( HR= 1.96; P |
【本文地址】